-

Rhidyll Moleciwlaidd JZ-ZMS3
-

Rhidyll Moleciwlaidd JZ-ZMS4
-

Rhidyll Moleciwlaidd JZ-ZMS5
-

Rhidyll Moleciwlaidd JZ-ZMS9
-

Powdwr Rhidyll Moleciwlaidd JZ-ZT
-

Rhidyll Moleciwlaidd JZ-AZ
- Disgrifiadau
- Mae moleciwlau gwahanol sylweddau yn cael eu gwahaniaethu gan flaenoriaeth a maint yr arsugniad, felly gelwir y ddelwedd yn "gogr moleciwlaidd".
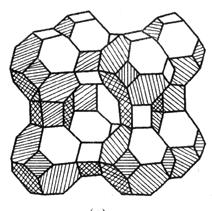
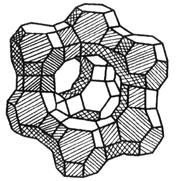
- Molecular sieve (also known as synthetic zeolite) is a silicate microporous crystal. Mae'n strwythur sgerbwd sylfaenol sy'n cynnwys silicon aluminate, gyda cations metel (fel Na +, K +, Ca2 +, ac ati) i gydbwyso'r gwefr negyddol gormodol yn y grisial. The type of molecular sieve is mainly divided into A type, X type and Y type according to its crystal structure.
|
| Mx/n [(alo.222O. |
|
|
|
|
|
|
| H2o |
|
| Nodweddion |
|
| Teipiwch ridyll amoleciwlaidd | | Prif gydran gogr moleciwlaidd Math A yw silicon aluminate. The main crystal hole is octaring structure.The aperture of the main crystal aperture is 4Å(1Å=10-10m), known as type 4A (also known as type A) molecular sieve; Cyfnewidiwch y CA2 + am y Na + yn y rhidyll moleciwlaidd 4A, gan ffurfio agorfa o 5A, sef rhidyll moleciwlaidd math 5A (aka calsiwm A); K + ar gyfer gogr moleciwlaidd 4A, gan ffurfio agorfa o 3A, sef moleciwlaidd 3A (aka potasiwm A). |
|
|
| Prif gydran y gogr moleciwlaidd x yw silicon aluminate, y prif dwll crisial yw deuddeg strwythur cylch elfen. Mae strwythur grisial sy'n ffurfio yn ffurfio grisial gogr moleciwlaidd gydag agorfa o 9-10 a, o'r enw 13x (a elwir hefyd yn sodiwm x math) molecular molecular molecular ostyngiad; crystal with a aperture of 8-9 A, called a 10X (also known as calcium X) molecular sieve. |
- Nghais
- Mae dosbarthiad agorfa'r gogr moleciwlaidd yn unffurf iawn, a dim ond sylweddau â diamedr moleciwlaidd sy'n llai na diamedr y twll sy'n gallu mynd i mewn i'r twll crisial y tu mewn i'r gogr moleciwlaidd.